今日の講義の内容
まず理想気体の場合の内部エネルギーが温度だけで決まるという話から。
理想気体を断熱状態で体積$V$から$V'$へ、真空に向けて膨張させたとする。このとき、膨張するが仕事はしないので、内部エネルギーは変化しない。理想気体ではこのとき温度が下がらないので、理想気体の場合の内部エネルギーを、$T,V$の関数として表現すると$V$にはよらないことがわかる。
ここでふと思い出したので、だいぶ前の琉大入試問題を聞いてみた。
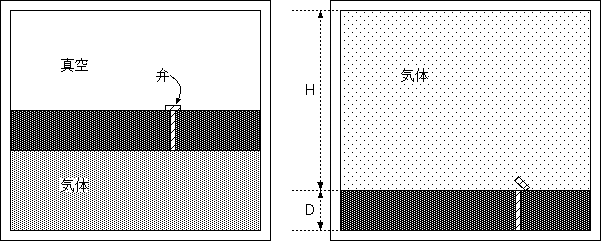
上のように断熱されたピストンの上を真空、下に理想気体を入れる。栓を抜いて気体が移動できるようになると、右のようにピストンが落ちた状態になる。
このとき理想気体の温度はどうなるだろう?
- 真空相手なら仕事はしないから、温度は変わらない。
- 断熱膨張しているんだから温度は下がる。
- ピストンが下がった分、ピストンの位置エネルギーを気体がもらって、温度が上がる。
の三つから選んでもらったら(上の話の直後にもかかわらず)、解答がバラけた。
これは3.が正解で、気体の圧力はピストンを上向きに持ち上げようとするが実際にはピストンが下に動くので、この場合気体はマイナスの仕事をしている。マイナスの仕事をすればエネルギーが増える、ということで$U$が増加、つまり温度が高くなる。
さて、理想気体の内部エネルギーがどんな関数かというと、 $$ U=cNRT + Nu $$ となる。$Nu$の部分は「$T$で微分すると消える部分(いわば$\left({\partial U(T;X)\over \partial T}\right)_X=cNR$を積分したときの積分定数)」である($V$の変数でもない)。$U$が示量変数だから、$N$に比例することがわかる($N^2$とか${1\over N}$に比例する項はない)。$u$の意味はずっと後でやる。
理想気体を断熱操作した場合、$U$が$V$によらないから$U$の変化は${\partial U\over \partial T}\mathrm dT$になり、そのときする仕事$P\mathrm dV$は(状態方程式を使って${NRT\over V}\mathrm dV$となる。よって、
$$cNR \mathrm dT = - {NRT\over V}\mathrm dV$$という微分方程式を解いて、
$$ c \log T = - \log V+A$$($A$は積分定数)より、$ T^c V=$(一定)という答が出る。
熱の定義
以上で等温操作と断熱操作についてある程度説明が終わったので、この二つを、「出発点と到着点が同じ操作」について比較してみる。つまり、等温準静的操作で $$ (T;V){{\rm iq}\atop \leftarrow}(T;V') $$ という変化(このとき、系は外部に$W_{\rm max}$の仕事をしたとする)と、断熱(準静的でなくてよい)操作で $$ (T;V){{\rm a}\atop \leftarrow}(T;V') $$ という変化この操作は実現しない可能性がある。その場合はこの「逆の操作」を考える。(このとき、系は外部に$W_{\rm ad}$の仕事をしたとする)を比較する。
前者でのする仕事は「環境からの影響を受けながらの仕事」で後者では「環境から切り離されての仕事」になる。膨張する場合、前者の方が大きいが、それは「環境からの補給を受けながら仕事をした」と考えることができる。その「エネルギーの補給」にあたるものが熱で、それを$Q_{\rm max}$と書く。$W_{\rm ad}$は内部エネルギーの変化だから、 $$ W_{\rm max}=U(T;V)-U(T;V')+Q_{\rm max} $$ となる。
こうして「熱」が定義できた。エネルギーの変化量のうち、$P\mathrm dV$などの形で「目に見えるもので計算できる部分(仕事)」を除いた、「目に見えない形でのエネルギーの移動」が熱だと思ってもよい。
最後に、
で遊びつつ、カルノーサイクルの意味について説明した。
カルノーサイクルは高温熱源から熱をもらって低温熱源に放出し、その差の分だけ仕事をするメカニズムである。吸熱を$Q_{\rm in}$、排熱を$Q_{\rm out}$とすると、仕事は$W=Q_{\rm in}-Q_{\rm out}$となるから、仕事を多くしたいなら、$Q_{\rm out}$を少なくしたい。しかしこれは0にはできない。0だとすると一つの熱源からもらう熱で正の仕事ができてしまい、Kelvinの原理に反するのである。
それでもできるだけ$Q_{\rm out}$を小さくしたいところであるが、${Q_{\rm out}\over Q_{\rm in}}$の値は実は二つの熱源の温度だけで決まり、${Q_{\rm out}\over Q_{\rm in}}={T_{\rm out}\over T_{\rm in}}$のような式が成立している、というのがカルノーの原理である。
来週はカルノーの原理の証明から行こう。